Atomic Structure
परमाणु संरचना
Previous Year Questions
Note:- प्रीवियस ईयर के questions रिपीट होते हैं तो इसे ध्यान से पढ़ें
1. एक गर्म फिलामेंट से निकली इलेक्ट्रॉन धारा कोे Vesu के विभवान्तर पर रखे
दो आवेशित प्लेटों के बीच से भेजा जाता है। यदि इलेक्ट्रॉन के आवेश तथा
संहति क्रमशः e तथा m हो तो h/λ का मान निम्न में से किसके द्वारा दिया
जाएगा? (जब इलेक्ट्रॉन तरंग से सम्बन्धित तरंगदैध्र्य λ है) (JEE 2016)
(a) 
(b) 
(c) 
(d) 
2. निम्नलिखित में से हाइड्रोजन की सम्भव उत्तेजित अवस्था की उर्जा कौन-सी है? (JEE 2015)
(a) + 13.6 eV
(b) - 6.8 eV
(c) - 3.4 eV
(d) + 6.8 eV
3. रूबिडियम परमाणु (Z = 37) के लिए संयोजी इलेक्ट्रॉनों के उचित चार क्वाण्टम संख्याओं का समूह होता है (JEE 2014)
(a) 5, 0, 0, +1/2
(b) 5, 1, 0, +1/2
(c) 5, 1, 1, +1/2
(d) 5, 0, 1, +1/2
4. एक इलेक्ट्रॉन की ऊर्जा को इस प्रकार प्रस्तुत किया जाता है  जूल
जूल )
प्रकाश की तरंगदैध्र्य हाइड्रोजन परमाणु में एक इलेक्ट्रॉन को n = 1 से n = 2 स्तर पर उत्तेजित करने के लिए आवश्यक होगी ( जूल सेकण्ड तथा
जूल सेकण्ड तथा  मी/से ) (JEE 2013)
मी/से ) (JEE 2013)
प्रकाश की तरंगदैध्र्य हाइड्रोजन परमाणु में एक इलेक्ट्रॉन को n = 1 से n = 2 स्तर पर उत्तेजित करने के लिए आवश्यक होगी (
(a)  मी
मी
(b)  मी
मी
(c)  मी
मी
(d)  मी
मी
5. एक हाइड्रोजन परमाणु में द्वितीय बोर (Bohr) कक्षा में इलेक्ट्रॉन (electron) की गतिज ऊर्जा (Kinetic energy) है [a0 : बोर त्रिज्या (Bohr radius)] (JEE 2012)
(a) 
(b) 
(c) 
(d) 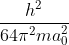
6. 54Fe, 56Fe तथा 57Fe समस्थानिकों का बहुलता (abundance) क्रमशः 5%, 90% और 5% है। Fe का परमाणु द्रव्यमान है (JEE 2009)
(a) 55.85
(b) 55.95
(c) 55.75
(d) 56.05
7.3s- तथा 2p-कक्षकों में त्रिज्य निस्पंदों (radial nodes) की संख्या क्रमशः है (JEE 2005)
(a) 2, 0
(b) 0, 2
(c) 1, 2
(d) 2, 11
8. निम्न में से किसकी त्रिज्या, हाइड्रोजन परमाणु की बोर त्रिज्या के समान होती हैं? (JEE 2004)
(a) n = 2, Li 2+
(b) n= 2, Be 3+
(c) n = 2, He +
(d) n = 3, Li 2+
9. परमाणु के नाभिकीय मॉडल की स्थापना में रदाफोर्ड के प्रयोग में निम्न किरण (beam) का प्रयोग किया गया (JEE 2002)
(a) ß-कण, जो धातु की पतली पन्नी से टकराकर अवशोषित हो जाते हैं
(b) ϒ-किरणें, जो धातु की पतली पन्नी से टकराकर इलेक्ट्रॉन उत्सर्जित करती हैं
(c) हीलियम के परमाणु, जो धातु की पतली पन्नी से टकराकर विक्षेपित हो जाते हैं
(d) हीलियम नाभिक, जो धातु की पतली पन्नी से टकराकर विक्षेपित हो जाता है
10. यदि नाइट्रोजन का इलेक्ट्रॉनिक विन्यास 1s7 होता, तो इसकी उर्जा, मूल अवस्था के इलेक्ट्रॉनिक विन्यास 1s2, 2s2,2p3 से कम होती, क्योंकि इलेक्ट्रॉन नाभिक के अधिक निकट होते, परंतु फिर भी 1s7 इलेक्ट्रॉनिक विन्यास नहीं पाया जाता है, क्योंकि यह झूठलाता है (JEE 2002)
(a) हाइजेनबर्ग का अनिश्चितता का सिद्धांत
(b) हुण्ड का नियम
(c) पाउली का अपवर्जन नियम
(d) बोर की स्थिर कोश की परिकल्पना
11. किसी इलेक्ट्रॉन के चक्रण के लिए क्वाण्टम संख्याएँ (+1/2) तथा (-1/2) प्रदर्शित करती हैं (JEE 2001)
(a) इलेक्ट्रॉन के क्रमशः वामावर्त तथा दक्षिणावर्त घूर्णन को
(b) इलेक्ट्रॉन के क्रमशः दक्षिणावर्त तथा वामावर्त घूर्णन को
(c) इलेक्ट्रॉन के चुम्बकीय आघूर्ण की दिशा क्रमशः ऊपर तथा नीचे होती है
(d) क्वाण्टम यान्त्रिकी चक्रण की दो अवस्थाओं को, जो अनुरूप नहीं हों
12. 5 मी/घण्टा की गति से घूमती हुई 200 ग्राम की एक गोल्फ गेंद (golf-ball) का तरंग दैर्ध्य है (JEE 2001)
(a) 10 - 10 मी
(b) 10 - 20 मी
(c) 10 - 30 मी
(d) 10 - 40 मी
13. px - कक्षक में नोडल तलों (nodal planes) की संख्या हैं (JEE 2000)
(a) 1
(b) 2
(c) 3
(d) 0
14. एक तत्व का इलेक्ट्रॉनिक विन्यास  है। यह प्रदर्शित करता है
है। यह प्रदर्शित करता है
(a) उत्तेजित अवस्था (JEE 2000)
(b) मूल अवस्था
(c) धनायन
(d) ऋणायन
15. हाइड्रोजन
परमाणु की प्रथम बोर कक्षा में उपस्थित एक इलेक्ट्रॉन की ऊर्जा -13.6 eV
है हाइड्रोजन परमाणु की बोर कक्षा में इलेक्ट्रॉन की उत्तेजित अवस्था की
सम्भावित ऊर्जा का मान है (JEE 1985)
(a) - 3.4 eV
(b) - 4.2 eV
(c) - 6.8 eV
(d) + 6.8 eV
16. किसी d- इलेक्ट्रॉन के लिए कक्षक कोणीय संवेग होता है (JEE 1997)
(a)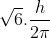
(b) 
(c) 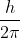
(d) 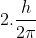
17. परमाणु की संरचना की व्याख्या करने के लिए क्वाण्टम सिद्धान्त का प्रयोग सर्वप्रथम किया था (JEE 1997)
(a) हाइजेनबर्ग ने
(b) बोर ने
(c) प्लांक ने
(d) आइन्स्टीन ने
18. निम्न में से किसमें अयुग्मित इलेक्ट्रॉनों की संख्या अधिकतम है? (JEE 1996)
(a) Mg2+
(b) Ti3+
(c) V3+
(d) Fe2+
19. 2s-कक्षक में उपस्थित एक इलेक्ट्रॉन का कक्षक कोणीय संवेग होगा (JEE 1996)
(a) 
(b) शून्य
(c) 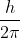
(d) 
20. निम्न में से कौन फोटाॅन की तरंग गति तथा कणों की धारा, दोनों से सम्बन्धित है? (JEE 1992)
(a) व्यतिकरण (interference)
(b) E=mc2
(c) विवर्तन (diffraction)
(d) E=hv
21. निम्न में से कौन-सा x-किरणों का गुण नहीं है? (JEE 1992)
(a) ये गैसों को आयनीकृत कर सकती हैं
(b) ये ZnS की प्रतिदीप्त का कारण हैं
(c) ये विद्युत तथा चुम्बकीय दोनों क्षेत्रों द्वारा विक्षेपित हो जाती हैं
(d) इनका तरंग-दैध्र्य पराबैंगनी किरणों से छोटा होता है
22. क्रोमियम परमाणु का मूल अवस्था में इलेक्ट्राॅनिक विन्यास है (JEE 1989)
(a) [Ar] 3d5 , 4s1
(b) [Ar] 3d4 , 4s2
(c) [Ar] 3d6 , 4s0
(d) [Ar] 4d5 , 4s1
23. किसी इलेक्ट्रॉनिक संक्रमण (electronic transition) के लिए किसी स्पेक्ट्रम रेखा का तरंग-दैध्य व्युत्क्रमानुपाती होता हैं (JEE 1988)
(a) संक्रमण करने वाले इलेक्ट्रॉनों की संख्या के
(b) परमाणु के नाभिकीय आवेश के
(c) संक्रमण में प्रयोग होने वाले ऊर्जा-स्तरों की ऊजाओ के अंतर के
(d) संक्रमण करने वाले इलेक्ट्राॅन के वेग के
24. समन्यूट्रॉनिक (isotonic) नाभिकों का समूह है (JEE 1988)
(a) 

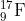
(b) 

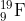
(c) 

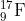
(d) 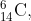


25.  तथा
तथा  तरंग दैर्ध्य वाले फोटाॅनों की ऊर्जाओं का अनुपात होगा (JEE 1986)
तरंग दैर्ध्य वाले फोटाॅनों की ऊर्जाओं का अनुपात होगा (JEE 1986)
(a) 1/4
(b) 4
(c) 1/2
(d) 2
26. रदरफोर्ड के ऐल्फा कण प्रकीर्णन प्रयोग से यह निष्कर्ष निकलता है कि (JEE 1986)
(a) द्रव्यमान तथा ऊर्जा सम्बंन्धित हैं
(b) नाभिक के चारों ओर के स्थान में इलेक्ट्रॉन रहते हैं
(c) नाभिक में न्यूट्रॉन होते हैं
(d) पदार्थ के साथ टक्कर का लक्ष्य ठीक प्रकार से ज्ञात किया जा सकता है
27. अधिकतम तरंग दैर्ध्य वाला विद्युत-चुम्बकीय विकिरण है (JEE 1985)
(a) पराबैंगनी (UV) विकिरण
(b) रेडियो तरंगें
(c) x - किरणें
(d) अवरक्त (infra-red) किरणें
28. परमाणु नाभिक की त्रिज्या होती है (JEE 1985)
(a) 10 - 10 सेमी
(b) 10 - 13 सेमी
(c) 10 - 15 सेमी
(d) 10 - 8 सेमी
29. बोर मॉडल व्याख्या कर सकता हैं (JEE 1985)
(a) केवल हाइड्रोजन परमाणु के स्पेक्ट्रम की
(b) केवल एक इलेक्ट्रॉन वाले परमाणु अथवा आयन के स्पेक्ट्रम की
(c) हाइड्रोजन अणु के स्पेक्ट्रम की
(d) सौर (solar) स्पेक्ट्रम की
30. निम्न
में से कौन-सा उर्जा-स्तर हाइड्रोजन परमाणु को फोटाॅन अवशोषित करने की
अनुमति देता है, परंतु फोटाॅन उत्सर्जित करने की अनुमति नहीं देता? (JEE 1984)
(a) 3s
(b) 2p
(c) 2s
(d) 1s
31. रूबिडियम (Rb37 ) के संयोजी इलेक्ट्रॉन के लिए चारों क्वाण्टम संख्याओं के मान होंगे (JEE 1984)
(a) 5, 0, 0, + 1/2
(b) 5, 1, 0, + 1/2
(c) 5, 1, 1, + 1/2
(d) 6, 0, 0, + 1/2
32.
इलेक्ट्रॉन (e), प्रोटॉन (p), न्यूट्रॉन (n) तथा ऐल्फा कण (α) के लिए आवेश
तथा द्रव्यमान के अनुपात (e/m) का बढ़ता हुआ क्रम (निम्नतम् से शुरू) है (JEE 1984)
(a) e, p, n, α
(b) n, p, e, α
(c) n, p, α, e
(d) n, α, p, e
33. रदरफोर्ड का प्रकीर्णन प्रयोग (scattering experiment) निम्न में से किसके आकार से सम्बन्धित है? (JEE 1983)
(a) नाभिक
(b) परमाणु
(c) इलेक्ट्रॉन
(d) न्यूट्रॉन
34. किसी परमाणु की मुख्य क्वाण्टम संख्या का सम्बंध है (JEE 1983)
(a) कक्षक के आकार से
(b) चक्रण कोणीय संवेग से
(c) कक्षक के अभिविन्यास (orientation) से
(d) कक्षक कोणीय संवेग से
35. एक p-कक्षक में हो सकते हैं (JEE 1983)
(a) चार इलेक्ट्रॉन
(b) छः इलेक्ट्रॉन
(c) समान चक्रण वाले दो इलेक्ट्रॉन
(d) विपरीत चक्रण वाले दो इलेक्ट्रॉन
Answer
| 1. | (c) |
| 2. | (c) |
| 3. | (a) |
| 4. | (a) |
| 5. | (c) |
| 6. | (b) |
| 7. | (a) |
| 8. | (b) |
| 9. | (d) |
| 10. | (c) |
| 11. | (d) |
| 12. | (c) |
| 13. | (a) |
| 14. | (b) |
| 15. | (a) |
| 16. | (a) |
| 17. | (b) |
| 18. | (d) |
| 19. | (b) |
| 20. | (d) |
| 21. | (c) |
| 22. | (a) |
| 23. | (c) |
| 24. | (a) |
| 25. | (d) |
| 26. | (b) |
| 27. | (b) |
| 28. | (b) |
| 29. | (b) |
| 30. | (d) |
| 31. | (a) |
| 32. | (d) |
| 33. | (a) |
| 34. | (a) |
| 35. | (d) |

CommentsEmoticon